Giản đồ pha và giản đồ sắt cacbon
Giản đồ trạng thái Fe-C
Hợp kim có thể tồn tại ở các pha khác nhau. Pha là trạng thái vật lý đồng nhất của hợp kim. Một pha có thành phần hóa học và sắp xếp các nguyên tử chính xác. Cấu trúc các nguyên tử sẽ đặc trưng cho tính chất của các pha. Chúng ta có thể lựa chọn các tổ chức bao gồm các pha với các ứng dụng khác nhau.
Chỉ một số hợp kim đặc biệt mới tồn tại được ở dạng đa pha. Quá trình nhiệt luyện làm thay đổi đổi tổ chức pha trong vật liệu.
Nội dung chính
Giản đồ pha là gì?
Giản đồ pha là một hình vẽ cho biết mối quan hệ giữa các pha trong hợp kim trong mối quan hệ với nhiệt độ, áp suất và thành phần nguyên tố
Giản đồ pha mô tả điều kiện phù hợp để tồn tại hai hoặc nhiều pha hơn tồn tại cân bằng. Ví dụ, giản đồ pha của nước mô tả một điểm haowcj ba điểm mà nước có thể cùng tồn tại trong một khoảng thời gian. Tại đây xảy qua trên nhiệt độ kết tinh 0,01 0.01°C ở 0,006 atm.
Sử dụng giản đồ pha
Dưới đây là bốn cách sử dụng chính giản đồ pha:
- Phát triển một hợp kim mới dựa trên những yêu cầu về ứng dụng
- Sản xuất các hợp kim này
- Phát triển và điều khiển quá trình nhiệt luyện để nâng cao tính chất hóa học, vật lý và cơ tính của hợp kim mới
- Giải quyết sự cố phát sinh trong ứng dụng những hợp kim mới này, cuối cùng là giải quyết khả năng dự đoán sản phẩm
Khi phát triển các hợp kim mới, giản đồ pha giúp giới hạn và ngăn chặn những thiết kế sai và không cần thiết cho các ứng dụng. Điều này giữ giá và thời gian quá trình sản xuất thấp. Chúng đồng thời phát triển hợp kim thay thế hoặc hợp kim tương tự với các nguyên tố thay thế. Nó có thể giúp giảm sử dụng các nguyên tố hiếm, độc và đắt tiền.
Tuổi đời của sản phẩm đồng thời được cải thiện khi giản đồ pha cho biết các vấn đề liên quan tới ăn mòn tinh giới, ăn mòn nóng và nguy cơ nguy hại của hidro.
Giản đồ Sắt cacbon
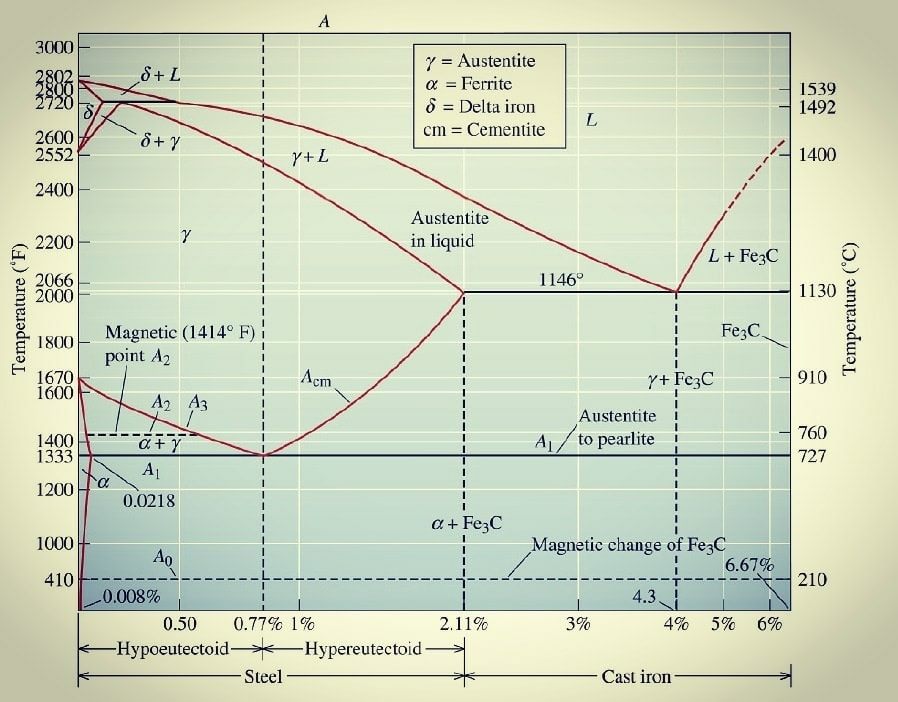
Dưới đây là hình ảnh giản đồ pha sắt và cacbon:

Giản đồ pha sắt cacbon được sử dụng phổ biến và là kiến thức cơ bản nhất cùng cường cong chữ C trong nghiên cứu nhiệt luyện gang và thép. Cả gang và thép đều là hợp chất của sắt và cacbon. Tùy vào thành phần cacbon sẽ chia ra làm gang và thép. Ngoài ra cả gang và thép đều chứa một lượng nhỏ các nguyên tố vi lượng./
Theo lý thuyết, giản đồ trạng thái Fe – C phải được xây dựng từ 100% Fe đến 100%C song do không dùng các hợp kim Fe – C với lượng cacbon nhiều hơn 5% nên ta chỉ xây dựng giản đồ đến 6,67% cacbon tức là ứng với hợp chất hóa học Fe3C. Giản đồ pha được vẽ với trục hoành (trục X) là thành phần của cacbon còn trục tung (trục Y) là trục nhiệt độ.
Cacbon tồn tại trong sắt dưới dạng xen kẽ. Hợp kim hình thành kiểu mạng lập phương tâm khối (FCC) và mạng lập phương tâm mặt BCC. Chúng sẽ hình thành nên dung dịch rắn α, γ, và δ.
Dưới đây là các đặc điểm chính của giản đồ Pha sắt- cacbon
Các tổ chức một pha
– Hợp kim lỏng (L): là dung dịch lỏng của cacbon trong sắt, tồn tại ở phía trên đường lỏng ABCD.
– Ferit (ký hiệu là F hay a): là dung dịch rắn xen kẽ của cacbon ở trong Fe(a), có mạng lập phương thể tâm nên khả năng hòa tan của cacbon ở trong Fe(a) là không đáng kể, lớn nhất ở 7270C là 0,02% và nhỏ nhất ở nhiệt độ thường là 0,006%.
– Austenit (kí hiệu là As hay g): là dung dịch rắn xen kẽ của cacbon trong Fe(g), có mạng lập phương diện tâm nên khả năng hòa tan cacbon của Fe(g) khá lớn, lớn nhất ở nhiệt độ 11470C với 2,14% và nhỏ nhất ở 7270C với 0,8%C.
Austenit rất dẻo và dai khi các nguyên tố khác hòa tan vào không những làm độ cứng tăng lên và độ dẻo độ dai giảm đi đáng kể mà còn làm thay đổi động học chuyển biến do đó ảnh hưởng lớn tới nhiệt luyện.
– Xementit (ký hiệu là Xe hay Fe3C): là hợp chất hóa học của sắt với cacbon – Fe3C có 6,67%C, ứng với đường thẳng đứng DFK.
– Xementit thứ nhất (XeI): là loại kết tinh từ hợp kim lỏng, nó được tạo thành trong các hợp kim chứa nhiều hơn 4,3% và trong khoảng nhiệt độ (1147 ¸ 1600)0C. Do tạo nên từ pha lỏng và ở nhiệt độ cao nên XeI có tổ chức hạt to.
– Xementit thứ hai (XeII): là loại được tiết ra từ dung dịch rắn Austenit ở trong khoảng nhiệt độ (727 ¸ 1147)0C khi độ hòa tan của cacbon ở trong pha này giảm từ 2,14% xuống còn 0,8% do vậy XeII có trong hợp kim với thành phần cacbon lớn hơn 0,8%. Do tạo từ pha rắn và ở nhiệt độ không cao lắm nên XeII có tổ chức hạt nhỏ hơn, do được tiết ra từ Austenit nên thường ở dạng lưới bao quanh Austenit.
– Xemetit thứ ba (XeIII): là loại được tiết ra từ dung dịch rắn Ferit ở trong khoảng nhiệt độ thấp hơn 7270C khi độ hòa tan giới hạn của cacbon trong Ferit giảm từ 0,02% xuống 0,006%. XeIII có ở trong mọi hợp kim có thành phần cacbon lớn hơn 0,006% nhưng với lượng rất ít. Do tạo nên từ pha rắn và ở nhiệt độ thấp, khả năng khuếch tán của nguyên tử rất kém nên XeIII thường ở dạng mạng lưới hay hạt rất nhỏ bên cạnh Ferit.
Các dạng Xementit không khác nhau về bản chất pha, chỉ khác nhau về kích thước hạt và sự phân bố do điều kiện tạo thành khác nhau.
Các tổ chức 2 pha
– Peclit (ký hiệu là P hay [a+Xe]): Peclit là hỗn hợp cơ học cùng tích của Ferit và Xementit ( tạo thành ở 7270C từ dung dịch rắn Austenit chứa 0,8%C. Trong Peclit có 88% Ferit và 12% Xementit. Từ giản đồ trạng thái Fe – C ta thấy trong quá trình làm nguội, thành phần cacbon của Austenit sẽ biến đổi và khi đến 7270C có 0,8%C sẽ chuyển biến thành hỗn hợp cùng tích của Ferit và Xementit:
Tùy theo hình dạng Xementit ở trong hỗn hợp, người ta chia ra 2 loại peclit là peclit tấm và peclit hạt (Peclit tấm Xementit ở dạng tấm phiến còn Peclit hạt thì Xementit ở dạng hạt). Peclit là hỗn hợp cơ học nên có tính chất trung gian. Kết hợp giữa tính dẻo, dai của Ferit và cứng, dòn của Xementit nên nói chung Peclit có độ cứng, độ bền cao, tính dẻo dai thấp. Tuy nhiên cơ tính của nó có thể thay đổi trong phạm vi khá rộng phụ thuộc vào độ hạt của Xementit.
– Ledeburit (ký hiệu là Le): Ledeburit là hỗn hợp cơ học cùng tinh, kết tính từ pha lỏng có nồng độ 4,3%C ở 11470C.
Lúc đầu mới tạo thành nó gồm Austenit và Xementit (trong khoảng 7270C ¸ 11470C). Khi làm nguội xuống dưới 7270C, g chuyển biến thành Peclit do vậy Ledeburit là hỗn hợp cơ học của Peclit và Xementit. Như vậy cuối cùng Ledeburit cũng có 2 pha là Ferit và Xementit trong đó Xementit chiếm tỉ lệ gần 2/3 nên Ledeburit rất cứng và dòn.
Quá trình kết tinh của hợp kim Fe-C
Phần phía trên đường đặc
– Khu vực có thành phần (0,1 ¸ 0,51) %C:
Khi làm nguội đến đường lỏng , hợp kim lỏng sẽ kết tinh ra dung dịch rắn d trước. Khi hạ nhiệt độ xuống tới 14990C, hợp kim có 2 pha là dung dịch rắn d chứa 0,1%C và dung dịch lỏng chứa 0,51%C nên xảy ra phản ứng bao tinh tạo ra dung dịch rắn Austenit chứa 0,16%C.
d0,1%C + L0,51%C g0,16%C
– Khu vực có thành phần (0,51 ¸ 4,3) %C:
Khi làm nguội hợp kim tới đường lỏng nó sẽ kết tinh ra Austenit. Các hợp kim có thành phần từ (0,51 ¸ 2,14) %C kết thúc kết tinh bằng sự tạo thành dung dịch rắn Austenit còn các hợp kim có thành phần từ (2,14¸ 4,3) %C kết thúc kết tinh bằng sự kết tinh của dung dịch lỏng có thành phần ứng với điểm C tạo ra 2 pha g có thành phần ứng với điểm E và Xementit ở 11470C.
Lc (gE + XeF)
Phần phía dưới đường đặc
Tại 7270C g có thành phần 0,8%C sẽ chuyển biến thành Peclit là hỗn hợp của 2 pha Ferit và Xementit gọi là hỗn hợp cơ học cùng tích.
gs [aR + XeK]
Như vậy trong bài này chúng tôi đã trình bày một kiến thức rất quan trọng liên quan tới vật liệu là giản đồ Pha. Tuy nhiên đây là những điểm chính, để hiểu nó bạn cần bỏ thời gian nghiên cứu và tìm tòi.

 日本語
日本語 English
English 中文 (中国)
中文 (中国)